Quelle physique explique la sono-cristallisation ?
Cette partie vise à apporter des éléments de compréhension des mécanismes physiques fondamentaux qui sous-tendent le processus de sono-cristallisation.
Les ultrasons provoquent divers effets physiques dans le milieu liquide dans lequel ils se propagent. Parmi eux, le phénomène de cavitation est le plus important, car il peut conduire à la génération, à la croissance et à l'effondrement de bulles de gaz, mais il peut aussi donner lieu à des phénomènes de micro-mélanges ou des collisions. Cela peut favoriser la nucléation du solide, ou améliorer les processus de transfert de chaleur et de matière à l'interface. En outre, les cristaux déjà formés peuvent se fractionner lorsqu'ils sont soumis à une onde de choc acoustique. Tous ces phénomènes affectent la distribution de taille des cristaux dans le produit final.
Les mécanismes de la nucléation
L'effet des ultrasons sur la nucléation est généralement attribué à la présence de bulles de cavitation, mais le mécanisme précis à l'échelle de la bulle n'a pas encore été mis en évidence expérimentalement. Par contre, différents mécanismes théoriques, qualitatifs ou semi-quantitatifs, à l'échelle de la bulle ont été proposés :
Rapide refroidissement local dû à l'expansion de la bulle ( Ruecroft et al., 2005a[1]), conduisant à une augmentation locale de sursaturation dans le cas où le soluté présente une solubilité qui augmente avec la température ;
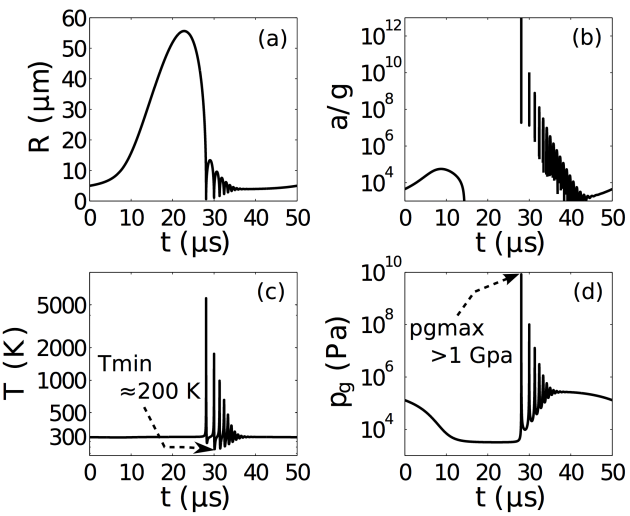
Haute pression jusqu'à un GPa lorsque la bulle s'effondre (figure ci-dessous) ( Virone et al., 2006[2], Grossier et al., 2007[3]) créant une sursaturation élevée, dans le cas où la solubilité du soluté diminue avec la pression ;
Effet chimique: formation de radicaux dans les bulles et au niveau des points chauds dans la solution ( Suslick et al., 1990[4]) ;
Accroissement du coefficient apparent de diffusion ( Guo et al., 2006, Li et al, 2006[6][5]);
Ségrégation inertielle par l'accélération dans le liquide des solutés et des précurseurs cristallins, pendant une très courte période de temps, ce qui modifie la nucléation ( Grossier et al., 2007[3]).
Les deux premiers phénomènes ont un effet thermodynamique en modifiant la sursaturation (ou la surfusion dans les milieux fondus). Les deux derniers phénomènes sont des effets cinétiques et sont reliés au mécanisme d'agrégation des molécules ou des ions impliqués dans la formation de la phase solide.
Nous allons examiner plus précisément ces différentes propositions.
L'effet thermodynamique
La pression et la température sont la force motrice de cristallisation (voir le contenu du cours sur la Sursaturation[8]).
Une forte réduction des temps d'induction a été observée pour différents cristaux sous ultrasons : c'est le cas par exemple pour le sulfate de potassium ( Lyczko et al., 2002[9]), pour la glycine ( Louisnard et Espitalier, 2007[10]), et pour le sulfate de zinc ( Harzali et al., 2012[11]). Les deux premiers constituants sont moins denses dans la phase solide que sous forme de soluté, en revanche pour le sulfate de zinc heptahydraté, les volumes moléculaires du soluté et du solide sont très proches. Dans ces trois cas, la forte augmentation de la pression au niveau de la paroi de la bulle lors de l'effondrement de celle-ci ne peut pas expliquer la diminution observée du temps d'induction. La réduction du temps d'induction que l'on observe expérimentalement avec de tels cristaux démontre que l'effet de la seule pression ne peut pas expliquer les résultats expérimentaux.
Le même raisonnement vaut pour la température. En effet, si la température diminue pour un solide dont la solubilité augmente avec la température, le rapport de sursaturation augmente. La forte réduction de la température observée dans la bulle pourrait conduire à une baisse de quelques degrés dans le liquide au voisinage de la bulle. Une légère diminution de la température pourrait alors induire une augmentation du taux de nucléation. Afin de vérifier cette hypothèse, il est nécessaire de tester l'application d'ultrasons dans le cas d'un solide présentant une solubilité constante ou décroissante lorsque la température augmente. À ce jour, aucun résultat n'a été trouvé dans la littérature.
effet cinétique
Effet sur le coefficient de diffusion
Certains auteurs suggèrent que l'accélération de la diffusion (ou de la mobilité) des espèces en solution est la cause principale de la réduction du temps d'induction. L'augmentation du coefficient de diffusion apparent peut être due au micro-mélange induit par l'effondrement des bulles de cavitation ( Suslick et al., 1990[4]).
Ségrégation
D'autres auteurs ont examiné la ségrégation de clusters autour des bulles de cavitation. Une bulle inertielle est théoriquement capable de séparer des grosses molécules ou des nanoparticules d'un liquide hôte de masse volumique différente. Une espèce plus dense que le liquide va se raréfier, en moyenne, au voisinage de la paroi de la bulle et sera largement sur-concentrée pendant un temps très court à la fin de l'effondrement de la bulle ( Louisnard et al., 2007[12], Grossier et al., 2007[3]). Dans le cas où l'espèce est un soluté dans un état d'équilibre métastable, cette ségrégation peut favoriser les attachements des molécules de soluté pour former des clusters, et donc augmenter le taux de nucléation, comme couramment observé lors des essais expérimentaux de sono-cristallisation. Cet effet de ségrégation autour d'une bulle de cavitation a été quantifié analytiquement par une méthode de perturbation ( Louisnard et al., 2007[12]).

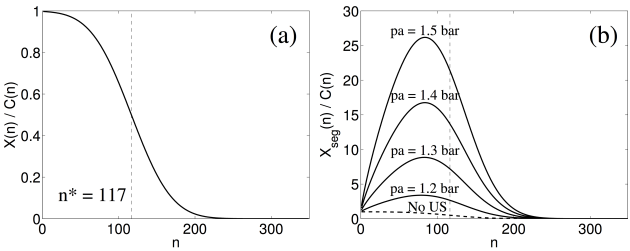
Sur cette base, il a été suggéré que, dans une solution métastable, cet effet devrait sur-concentrer les clusters près de la paroi de la bulle à chaque effondrement de celle-ci, favorisant ainsi leur collision directe, ce qui conduit à l'augmentation du taux global de nucléation. Pour examiner davantage cette hypothèse, la concentration des clusters, alors qu'ils se retrouvent ségrégés du liquide par le mouvement de la bulle, a été évaluée dans les conditions des expériences de cristallisation. Pour quatre amplitudes ultrasonores, la concentration des agrégats ayant des tailles comprises entre 1 et \(3n^*\), à proximité d'une bulle de cavitation inertielle typique, a été calculée pour le sulfate de zinc heptahydraté cristallisé par refroidissement ( Harzali et al., 2011[13]). La sur-concentration des clusters augmente lorsque l'amplitude ultrasonore augmente (figure ci-dessous). Il a été constaté que la ségrégation sur-concentre tous les agrégats, en particulier dans une région située en dessous du cluster critique (\(n^* = 117\)), jusqu'à plus de 20 fois pour une pression acoustique de 1,5 bar (courbe b). Selon la théorie de la nucléation, il est généralement supposé que, dans une solution sursaturée, les clusters changent de taille en raison de l'ajout ou de la perte de monomères, car la concentration des agrégats de plus grandes tailles est très faible ( Kashchiev, 2000[14]). Au voisinage de la bulle, les concentrations des clusters de \(n\)-tailles sont différentes, en raison de la ségrégation, de sorte que toutes les agrégations \(A_n + A_m \leftrightarrows A_{n+m}\) deviennent possibles.
Nucléation hétérogène
Il est communément admis que les bulles de cavitation générées agissent comme des particules étrangères, et que la nucléation est probablement favorisée par un mécanisme de nucléation hétérogène.
Mécanismes de croissance et d'attrition
En comparaison avec la nucléation, peu d'études présentent l'effet des ultrasons sur la croissance cristalline. Aucune tendance n'a été mise en évidence, contrairement à ce qui a été fait pour le temps d'induction ou pour la distribution de taille. Différentes hypothèses peuvent être formulées. Des cristaux sont brisées par la cavitation acoustique et, par conséquent certains de leurs fragments apparaissent en solution. Ces fragments induisent une augmentation de la surface disponible ce qui conduit à une augmentation du taux de cristallisation.
L'effondrement de la bulle près d'un solide peut induire un courant rapide de liquide avec des vitesses pouvant atteindre 100 m/s ( Suslick, 1989[16]). Ce courant liquide peut modifier l'intégration des unités de croissance dans le réseau cristallin. Deux cas sont présentés ci-dessous. Dans le cas du sulfate de baryum (figure ci-dessous), les cristaux croissent en présence d'ultrasons. Les ultrasons induisent une nucléation massive (contact secondaire) ( Gatumel et al., 1998[17]). En outre, des jets de liquide, lors de l'effondrement de la bulle, rendent difficile l'intégration des unités de croissance sur la face du cristal, ce qui modifie son faciès. Dans le cas du sulfate de potassium, les cristaux sont produits sous ultrasons, et leur croissance a lieu en conditions silencieuses ( i.e. sans ultrasons). Les cavités observées sur les faces cristallines (figure suivante) peuvent être créées par ces violents jets de liquide, empêchant l'intégration des unités de croissance et générant des défauts sur la surface des cristaux. Lorsque les cristaux se développent plus tard dans des conditions silencieuses, les faces conservent ces défauts.
Effets chimiques
Un tel effet a été observé par Dodds et al., 2007[20], lors de l'étude de la précipitation du \(\ce{TiO2}\) par thermo-hydrolyse du sulfate de titanyle. L'influence des gaz dissous est loin d'être évidente, mais cela a été examinée : il se trouve que le gaz dissous a un effet sur la forme cristalline résultante (anatase ou rutile). Les points chauds et la production de radicaux \(\ce{OH}\) lors de l'effondrement des bulles de cavitation pourraient alors expliquer les différentes structures de type polymères.