Exercice : Cas du Ritonavir
Le Ritonavir est une entité chimique utilisée dans le traitement du SIDA dont la structure chimique est donnée ci-dessous.
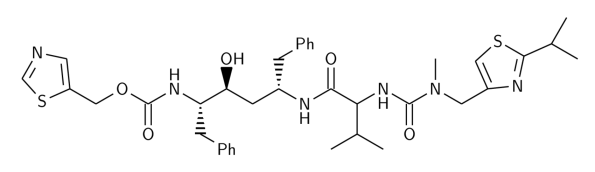
Durant toute la période de développement, seule une forme cristalline, nommée 1 avait été découverte. Beaucoup plus tard, une autre forme, dénommée 2 est apparue.
Les données ACD sont les suivantes :
\(T_{f,\,1} = 122\,°\textrm{C}\) | \(\Delta h_{f,\,1} = 78,2 \textrm{ J/g}\) |
\(T_{f,\,2} = 125\,°\textrm{C}\) | \(\Delta h_{f,\,2} = 87,8 \textrm{ J/g}\) |
Question
Quel type de relation thermodynamique existe entre les deux formes ?
Quelle est l'allure du diagramme \(G\left(T\right)\) correspondant ?
Solution
Selon la règle de fusion, le système est monotrope.
Cela signifie que la forme 2 est la plus stable thermodynamiquement dans tout le domaine de température (et pour le moins dans la zone de pression correspondant au point triple).
Question
La solubilité à +5 °C dans un mélange éthanol/eau (85/15) est de 234 mg/ml pour la forme 1 et de 61 mg/ml pour la forme 2.
Cela va-t-il dans le sens de la réponse que vous avez donnée à la question précédente ?
Calculer la différence d'énergie libre entre les deux formes à cette température.
Solution
Oui, cela est cohérent puisque la forme 1 est la forme instable, donc de plus haute énergie libre :c'est donc la forme 1 qui possède la solubilité la plus grande. La différence d'énergie libre entre forme 1et forme 2 est :
car
Remarque :
Dans cet exemple, le rapport des solubilités entre les deux formes est important. On peut être en droit de s'attendre à une différence de biodisponibilité entre les deux formes polymorphes.
Le produit avait été initialement commercialisé en utilisant la forme 1, la seule connue à l'époque. Quand la forme 2 plus stable est apparue, il a été impossible pendant un certain temps de reproduire la cristallisation de la forme métastable, et le produit pharmaceutique a dû être retiré du marché tant que le processus de cristallisation de la forme 1 n'était pas de nouveau maîtrisé. D'où l'importance du chapitre concernant la recherche a priori des formes polymorphes[3].