Exercice : Cas de l'Amibegron
Cette molécule a la structure suivante :
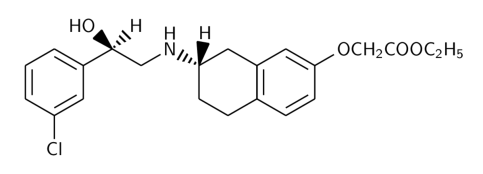
\({\rm M}_{\rm m}\) = 440,37 g/mol
Nous avons ici une entité chimique qui a été développée sous forme d'un sel, en l'occurrence un chlorhydrate.
Pour simplifier, nous supposerons que deux formes cristallines vraies, dénommées A et B, ont été identifiées dans le cadre du triage polymorphique. Les paramètres de mailles des deux formes sont donnés ci-dessous :
Forme A | Forme B | |
|---|---|---|
Formule chimique | \(\ce{C22H27N1O4Cl2}\) | \(\ce{C22H27N1O4Cl2}\) |
Poids moléculaire | 440,37 | 440,37 |
Système cristallin | orthorombique | orthorombique |
Groupe d'espace | P2,2,2 | P2,2,2 |
Paramètres de maille : \(a\ (Å)\) \(b\ (Å)\) \(c\ (Å)\) |
14,6119 14,7939 21,7429 |
6,5651 14,3500 22,8325 |
Z | 8 | 4 |
Volume (\(Å^3\)) | 4700 | 2151 |
Masse volumique (kg/m\(^3\)) | 1247 | 1360 |
Question
Quelle est la relation thermodynamique reliant \(A\) et \(B\) ?
Donner l'allure du diagramme \(G\left(T\right)\) pour les deux formes.
Votre réponse se trouve-t-elle confortée par l'examen des masses volumiques théoriques telles que présentées dans les tableaux ?
Solution
D'après la règle de la fusion, le système est énantiotrope.
Le diagramme \(G\left(T\right)\) est du type de celui représenté dans l'exercice concernant le Cas du F2692[3]. La forme \(B\) est la plus stable depuis le zéro absolu jusqu'à la température de transition solide-solide (qu'on ne connaît pas encore). Ceci est confirmé par la règle de la masse volumique qui précise que la forme la plus stable au zéro absolu est celle qui à la masse volumique la plus grande à la température ambiante (à laquelle l'étude RX[4] a été menée).
On effectue alors pour les deux formes une détermination des cinétiques de dissolution intrinsèques, soit \(J^A\left( T \right)\) et \(J^B\left( T \right)\) dans un milieu aqueux de\(pH=3\), avec une rotation de 100 tours/min et à 37 °C. La figure ci-dessous récapitule les données observées en \(\textrm{mg/cm}^2\) de produit dissout en fonction du temps.
Question
D'après ce résultat, quelle est la forme la plus stable à 37 °C ?
Cela vous permet-il de préciser un peu plus le diagramme \(G\left( T \right)\) tracé précédemment ?
Solution
On voit qu'à 37 °C, c'est la forme \(B\) qui est la plus stable puisqu'elle présente la cinétique de dissolution intrinsèque la plus petite.
On effectue cette même détermination à plusieurs températures et on trace ensuite un diagramme type Van't Hoff \(\ln \left( J \right) = f\left( \frac{1}{T} \right)\) pour les deux formes. On obtient les courbes suivantes :
On obtient un point de croisement pour la forme \(A\) (bleu) et la forme \(B\) (rouge) situé à une température de 63 °C.
Question
Cela vous permet-il de compléter votre connaissance de la thermodynamique du système ?
Sachant que les différences de cinétique de dissolution ne sont pas suffisamment importantes pour craindre un problème de bioéquivalence, quelle est la forme que vous choisiriez ?
Solution
Le fait que les courbes des cinétiques intrinsèques se coupent à 63 °C confirme le caractère énantiotrope du système et permet d'obtenir ainsi une estimation de la température de transition.
Puisqu'il n'y a pas d'avantage en terme de biodisponibilité, on aura intérêt à choisir la forme B la plus stable dans la zone de température correspondant à l'ambiante.
Question
Sachant qu'une granulation humide est prévue pour fabriquer un comprimé, ce qui implique un séchage vers 70 °C, quelle stratégie allez-vous mettre en place pour vous assurer que la forme cristalline choisie est bien celle présente en fin de fabrication ?
Solution
Au cours du séchage effectué vers 70 °C, il existe toujours un risque que la forme \(B\) se soit transformée en forme \(A\), au moins en partie. Il faudra donc vérifier à l'aide d'une méthode comme la diffraction des RX[4] que la forme \(B\) est toujours là après retour à la température ambiante.
Question
Les thermogrammes ACD[2] enregistrés cette fois à \(2\ \textrm{°C.min}^{-1}\) sont fournis ci-après. En fonction de la connaissance que vous avez maintenant du type de relation thermodynamique existant entre \(A\) et \(B\), comment interprétez-vous ceux-ci ?
(on précise que les évènements thermiques enregistrés ne comportent aucune transition solide-solide)
Solution
Le thermogramme de la forme \(B\) montre que le produit va dans ces conditions jusqu'à sa fusion (partie endothermique vers 125 °C), suivi immédiatement par la recristallisation (exotherme) en forme \(A\), qui va ensuite jusqu'à sa fusion (160 °C).
Pour la forme \(A\), le thermogramme montre que celle-ci peut être directement menée à sa fusion sans subir de transformation.
Comme nous l'avons dit dans le cours , il faut faire attention à ne pas se contenter des allures des tracés ACD[2] pour caractériser un système polymorphe. D'autres approches, comme nous l'avons vu, sont nécessaires pour compléter la connaissance des systèmes.